Forsøg med elektrolyse
FORSØG: Den nemmeste måde at fremstille hydrogen ved hjælp af elektricitet er ved elektrolyse. Det kan du selv prøve i dette forsøg.
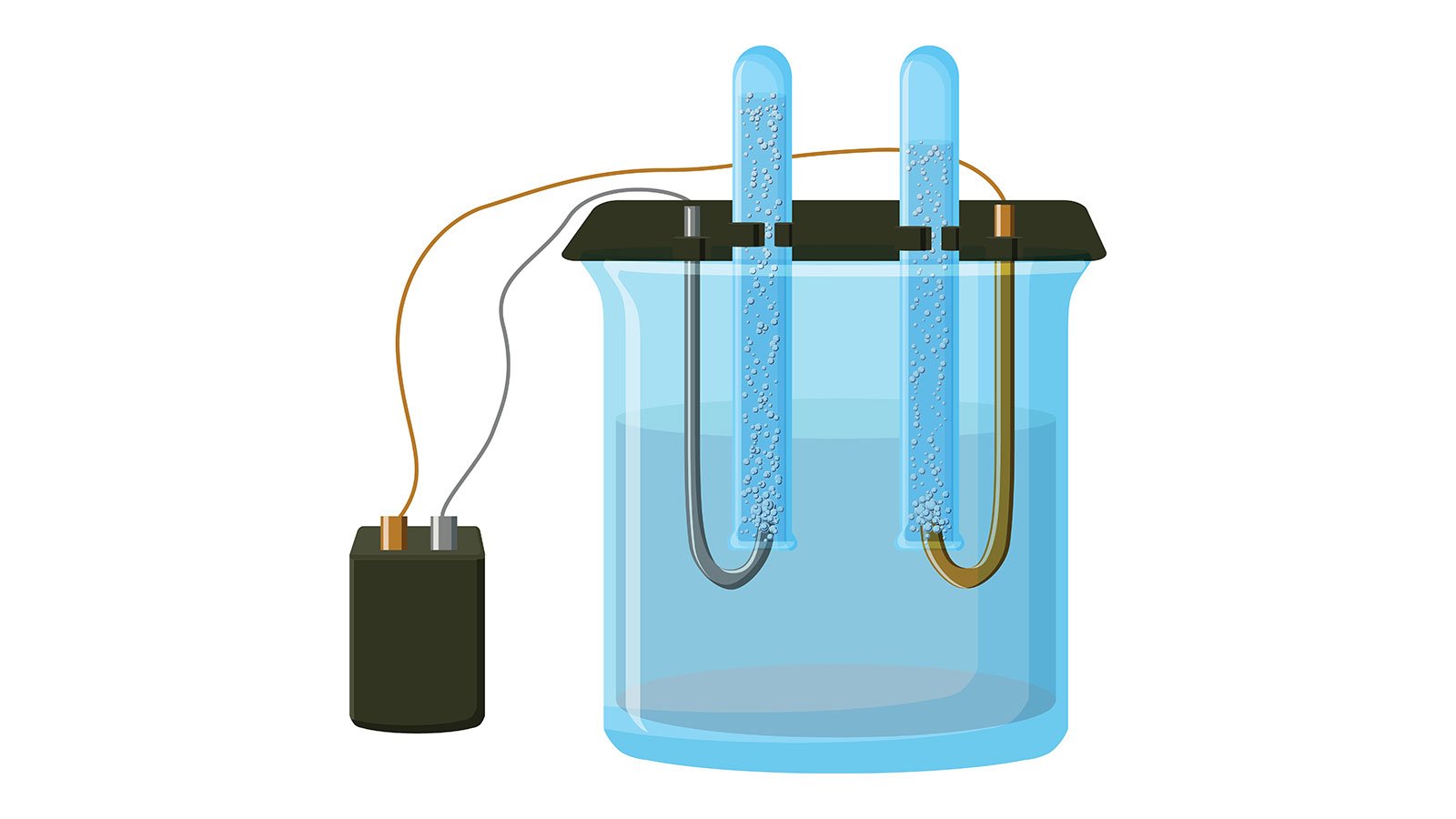
Den nemmeste måde at fremstille hydrogen ved hjælp af elektricitet er, som i dette forsøg, ved elektrolyse. Her sender man jævnstrøm gennem et kar med vand. Vandet skal være elektrisk ledende, så derfor tilsætter man fortyndet svovlsyre, fortyndet natriumhydroxid, saltvand eller lignende.
Når der sendes strøm gennem vandet, vil vandmolekylerne dissocieres (adskilles) i H+-ioner og OH–-ioner. Disse ioner trækkes hen mod henholdsvis den negative pol (katoden) og den positive pol (anoden).
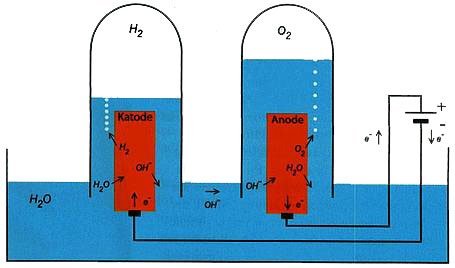
Ved katoden optager to H+-ioner hver en elektron og danner hydrogen (H2). Vi siger, at hydrogenionerne er blevet reduceret (reduktion = elektronoptagelse).
Ved anoden samles fire OH–-ioner og frigiver dels O2 (ilt), molekylært vand og fire elektroner. I denne proces afgives der elektroner fra oxidionerne i OH–. Der er sket en oxidation (oxidation = elektronafgivelse).
Katode (negativ): 4 H2O (l) + 4 e– → 2 H2 (g) + 4 OH– (aq)
Anode (positiv): 4 OH–(aq) → O2(g) + 4 e– + 2 H2O (l)
Det ses, at der efter nogen tid dannes gasser i reagensglassene. Det kan påvises, at disse gasser er hydrogen (H2) ved den negative elektrode og oxygen (O2) ved den positive elektrode, og at de bliver dannet i forholdet 2:1. Der er således sket en sønderdeling af vand, H2O.

Påvis CO2-udledning fra biler
Illustrationsforsøg af forbrændingsmotor
Forsøg med elektrolyse (denne side)
Byg din egen elmotor
Lav en simpel elektromotor
Lav et luftpudefartøj
Dette forsøg stammer oprindeligt fra Climate Minds, som er udviklet af Experimentarium i samarbejde med Dansk Energi og Energyminds.


